一、实验目标
1. 掌握双酚A型环氧树脂的实验室制法。
2. 了解环氧值的测定方法和一般环氧树脂胶粘剂的配制方法和应用。
二、产品特性与用途
凡是含有环氧基团的聚合物,总称为环氧树脂。环氧树脂品种很多,但以双酚A型环氧树脂综合性能最好,产量最大。双酚A型环氧树脂占环氧树脂总量的90%,也是在环氧胶粘剂中应用最普遍、工艺最成熟的一种环氧树脂,有通用环氧树脂之称。
双酚A型环氧树脂有低分子量、中等分子量和高分子量三种。双酚A型低分子量环氧树脂,学名双酚A二缩水甘油醚、E型环氧树脂,为黄色或琥珀色高粘度透明液体,软化点低于50℃,分子量小于700,易溶于二甲苯、甲乙酮等有机溶剂。
通常环氧树脂胶粘剂大多采用低分子量环氧树脂,而热熔胶采用高分子量环氧树脂。环氧树脂胶粘剂可不用溶剂直接粘接,具有粘接强度高、固化收缩小、耐高温、耐腐蚀、耐水、电绝缘性高、易改性、毒性小和使用范围广等优点,因此,在各个领域都得到了广泛应用,有“万能胶”之称。
三、实验原理
1. 双酚A型环氧树脂的合成原理
双酚A型环氧树脂由环氧氯丙烷与双酚A在氢氧化钠作用下聚合制得。
该反应为逐步聚合反应,通常认为它们在氢氧化钠存在的条件下,不断地进行环氧基开环和闭环的反应。即:

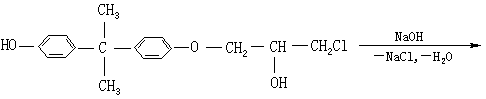

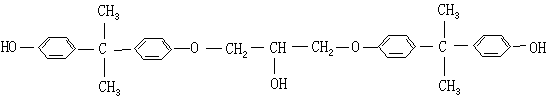
继续反应下去,即得长链分子,反应通式如下:

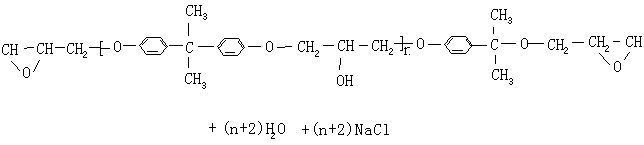 环氧基开环反应为放热反应,闭环反应为吸热反应。
环氧基开环反应为放热反应,闭环反应为吸热反应。
两种单体的配比与所得环氧树脂的分子量直接相关,环氧氯丙烷与双酚A的物质的量之比越接近于1,聚合度越高,分子量越大,产物的软化点越高;而环氧氯丙烷过量越多,越有利于形成末端环氧基,得到的环氧树脂分子量越低;另外,缩聚反应的温度、碱的用量及加料顺序对环氧树脂的分子量和结构也有影响。因此,控制不同的配料比和工艺条件,可制得不同规格的环氧树脂。本实验所制环氧树脂为低聚合度、高环氧值的品种,因此,在实验中使用过量的环氧氯丙烷。
2. 环氧值的测定
环氧值是指每100g树脂中所含环氧基的摩尔数。它是环氧树脂质量的重要指标之一,也是计算固化剂用量的依据。分子量越高,环氧基团间的分子链也越长,环氧值就越低。一般低分子量环氧树脂的环氧值在0.50~0.57之间。分子量小于1500的环氧树脂,其环氧值测定采用盐酸—丙酮法。反应如下:

过量的HCl用标准NaOH—C2H5OH溶液回滴。
3. 环氧树脂胶粘剂的粘接和固化机理
在环氧树脂结构中含有脂肪族羟基、醚基和极活泼的环氧基,羟基和醚基都有高度的极性,使环氧树脂分子能与临界面产生静电引力,而环氧基团与介质表面的游离基起反应形成化学键,所以环氧树脂的粘合力特别强。
环氧树脂在未固化前是呈热塑性的线形结构,使用时必须加入固化剂,固化剂与环氧树脂的环氧基等反应,变成网状结构的大分子,成为不溶不熔的热固性物质。
现以室温下即能固化的乙二胺为例,它是按下列反应进行:


该反应主要是利用线形环氧树脂分子两端的环氧基与胺分子上的活泼氢反应,使线形分子交联起来。
四、主要仪器与药品
1. 主要仪器
四口瓶、电动搅拌装置、滴液漏斗、分液漏斗、回流冷凝管、电热套、减压蒸馏装置一套、铝片。
2. 主要药品
双酚A、环氧氯丙烷、氢氧化钠、盐酸—丙酮溶液、氢氧化钠乙醇溶液、苯、乙二胺、酚酞试液、浓硫酸、重铬酸钾。
五、实验内容与操作步骤
1. 环氧树脂的制备
⑴ 将22 g双酚A(0.1 mol)、28 g环氧氯丙烷(0.3 mol)加入装有搅拌器、滴液漏斗、回流冷凝管及温度计的四口瓶中,搅拌并加热至70 ℃,使双酚A全部溶解。
⑵ 称取8 g氢氧化钠溶解在20 mL水中,置于60 mL滴液漏斗中;慢慢滴加氢氧化钠溶液至四口瓶中,保持反应液温度在70 ℃左右,约30 min内滴加完毕;在75~80℃继续反应1.5~2 h,可观察到反应混合物呈乳黄色。
⑶ 向反应瓶中加入30 mL蒸馏水和60 mL苯,充分搅拌,倒入分液漏斗,静止分层后,分去水层;油层用蒸馏水洗涤数次,直至分出的水相呈中性无氯离子。(用pH试纸和AgNO3溶液试验)
⑷ 先常压蒸馏,除去苯;然后减压蒸馏,以除去苯、水及未反应的环氧氯丙烷。得到淡黄色透明粘稠液。
2. 环氧值的测定
⑴ 用移液管将1.6 mL浓盐酸(ρ=1.19 g/mL)转入100 mL的容量瓶中,以丙酮稀释至刻度,配成0.2 mol/L的盐酸丙酮溶液(现配现用,不需标定)。
⑵ 在锥形瓶中准确称取0.3~0.5 g样品,准确吸取15 mL盐酸丙酮溶液移入锥形瓶。将锥形瓶盖好,放在阴凉处(约15 ℃的环境中)静置1h。然后加入两滴酚酞指示剂,用0.1 mol/L的标准NaOH溶液滴定至粉红色,做平行试验,并做空白对比。
3. 胶粘剂的配制和应用
本实验制得的是低分子量环氧树脂。应用试验时可用各种金属、玻璃、聚氯乙烯塑料、瓷片等作为试样。
粘接操作包括对被粘物的表面处理、粘合剂的配制、粘接和固化。
⑴ 表面处理 为保证胶粘剂与被粘接界面有良好的粘附作用,被粘接材料必须经过表面处理,以除去油污等杂质。
将两块铝片在处理液(K2Cr2O710份,浓硫酸50份,H2O340份)中浸泡10~15min,以除去油污,然后将其表面打磨,使其粗糙,蒸馏水冲洗,热风吹干,自然冷却至室温。
⑵ 粘合剂的配制 按如下配方配制粘合剂。
环氧树脂(本实验产品)10 g; 轻质碳酸钙(填料)6 g;
邻苯二甲酸二丁酯(增塑剂)0.9 g; 乙二胺(固化剂)0.8 g。
⑶ 胶接和固化:取少量涂于两块铝片端面,胶层要薄而均匀(约0.1mm厚),把两块铝片对准胶合面合拢,使用适当的夹具使粘接部位在固化过程中保持定位;室温下放置8~24 h可完全固化,1~4d后可达到最高的粘接强度,升温可缩短固化时间,例如在80℃,固化时间不超过3h。
六、实验记录与数据处理
1. 实验记录
环氧值测定中,试样质量: g;对照试验消耗NaOH溶液体积: mL;试样消耗NaOH溶液的体积: mL。
2.数据处理
⑴ 计算环氧值

式中 E——环氧树脂的环氧值;
cNaOH——NaOH溶液的浓度,mol/L;
V1——对照试验消耗的NaOH溶液的体积,mL;
V2——试样消耗的NaOH溶液的体积,mL;
m ——样品质量,g。
⑵ 计算固化剂胺的用量

式中 G——每100 g环氧树脂所需胺的质量,g;
M——胺的摩尔质量,g/mol;
H——胺中活泼氢原子的数目;
E——环氧树脂的环氧值。
本实验中乙二胺的摩尔质量M取 60.1 g/ mol;乙二胺中活泼氢原子的数目等于4。实际用量可在上述公式计算的基础上,再增加5%~10%。
七、安全与环保
1. 乙二胺有毒性、有臭味,挥发性大,对眼睛、呼吸道和皮肤均有刺激性,固化时放出大量热,宜在通风橱内进行相关操作。
2. 减压蒸馏后期,物料粘度较大且温度较高,应密切关注蒸馏烧瓶内的毛细管是否堵塞,以防发生事故。
八、思考题
1. 根据所得产品的实测环氧值计算粘合剂配方中乙二胺的用量。
2. 环氧树脂中加入固化剂的作用是什么?固化剂的用量对胶粘剂的性能有什么影响?
3. 本实验中所用氢氧化钠为什么缓慢滴加而不一次投入?